Currículum
Acceso a Medicina - Universidades privadas
FORO
0/1B1. Bioelementos y biomoléculas inorgánicas
0/3B2. Glúcidos
0/4B3. Lípidos
0/2B4. Proteínas
0/4Teoría Bioelementos y biomoléculas inorgánicas
1. BIOELEMENTOS
Los bioelementos son los elementos que forman parte de los seres vivos. Los podemos clasificar en:
• Bioelementos primarios. Representan alrededor del 96% del total, por lo que constituyen la práctica totalidad de las moléculas biológicas. Éstos son C, H, O, N, P, S.
• Bioelementos secundarios. Son los restantes. Hay dos tipos.
– Los indispensables no pueden faltar para la vida de la célula; son Na, K, Mg, Fe, Cl, etc.
– Los variables pueden faltar en algunos organismos; son Br, Zn, Pb, etc.
Los que se encuentran en proporciones menores al 0,1 % se llaman oligoelementos (los más universales son Fe, Cu, Zn, Mn, I, Ni, Co).
1.1. BIOELEMENTOS PRIMARIOS
Los altos porcentajes de H y O en la biosfera se deben a que la materia viva está constituida por agua. Esto se relaciona con que la vida se originó en el medio acuático.
Los porcentajes del resto de los bioelementos primarios de la biosfera son muy diferentes a los encontrados en litosfera, atmósfera e hidrosfera, por lo que no se puede deducir que la materia viva se haya formado a partir de los elementos más abundantes, sino de los que tienen unas propiedades capaces de constituirla:
– Masa atómica pequeña que favorece enlaces covalentes estables.
– El N y O son muy electronegativos y dan lugar a moléculas dipolares, que se pueden disolver en agua y pueden reaccionar entre sí.
El resto de las propiedades no son comunes:
a) 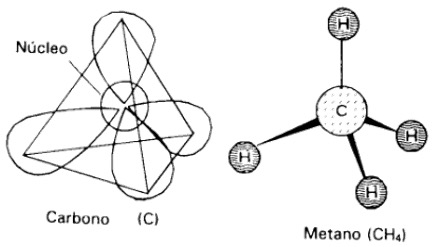 Carbono. Puede formar cuatro enlaces covalentes que le permiten constituir largas cadenas de átomos.
Carbono. Puede formar cuatro enlaces covalentes que le permiten constituir largas cadenas de átomos.
Los cuatro enlaces covalentes están dirigidos en el espacio hacia los cuatro vértices de un tetraedro imaginario. Esta estructura tetraédrica de los compuestos de carbono proporciona a las moléculas una configuración tridimensional de la que derivan sus múltiples funciones.
Los enlaces C-C son estables y forman largas y variadas cadenas carbonadas:
· Cadenas lineales con todo tipo de enlaces
· Cadenas ramificadas
· Cadenas cíclicas: cuando los extremos de la cadena aparecen unidos entre sí dando origen a estructuras cíclicas o anillos.
Por otro lado, gracias a que los enlaces pueden ser simples, dobles o triples, entre ellos o con los de hidrógeno, oxígeno, nitrógeno, azufre, etc., dan lugar a cantidad de grupos funcionales que pueden reaccionar entre sí y originar nuevas moléculas orgánicas con diversos grupos funcionales. Todo ello resulta útil para las continuas transformaciones que sufre la materia de los seres vivos en su metabolismo.
¿Por qué el carbono y no el silicio como base química de la vida?
Los enlaces C-C, C=O, y C-N son suficientemente fuertes y estables, y, a la vez, susceptibles de romperse sin excesiva dificultad. Esto permite al ser vivo obtener energía y almacenarla. En cambio, las cadenas de silicio son inestables, y las de silicio y oxígeno (siliconas) casi inalterables.
El CO2 es gaseoso y soluble en agua, por lo que puede circular a través de los seres vivos. Por el contrario, el SiO2 (sílice) es sólido e insoluble en agua.
b) Hidrógeno. Resulta indispensable para formar materia orgánica. Carbono e hidrógeno forman hidrocarburos.
El único electrón que posee le permite formar un enlace con cualquiera de los otros bioelementos primarios. Las moléculas formadas sólo por carbono e hidrógeno son covalentes apolares (insolubles en agua). Si algunos hidrógenos son sustituidos por grupos covalentes polares, la molécula orgánica puede llegar a ser soluble en agua.
c) Oxígeno. Es el bioelemento primario más electronegativo, lo que lo hace idóneo para quitar electrones (oxidar).
d) Nitrógeno. Forma compuestos tanto con el hidrógeno como con el oxígeno lo que permite la liberación de energía al pasar de una forma a otra. Forma aminoácidos y bases nitrogenadas.
Prácticamente todo el nitrógeno es incorporado al mundo vivo por algas y plantas que lo absorben en forma de ión nitrato.
e) Azufre. Se encuentra como radical sulfhidrilo en aminoácidos. Los puentes disulfuro (-S-S-) mantienen la estructura de las proteínas.
f) Fósforo. Establece enlaces ricos en energía e interviene en la constitución de los ácidos nucleicos.
1.2. BIOELEMENTOS SECUNDARIOS
- Abundantes: Na, K, Mg y Ca. En medio acuoso se encuentran siempre ionizados. Los iones Na+, K+ Cl– intervienen en el mantenimiento del grado de salinidad. El Na+ y el K+ son fundamentales en la transmisión del impulso nervioso. El calcio en forma de carbonato forma caparazones y esqueletos, y como ión actúa en la contracción muscular. El magnesio es un componente de la clorofila.
- Oligoelementos: Fe, Zn, Cu, Co, Mn, Li, Si, I y F. Son imprescindibles para la vida aunque no todos los seres vivos tienen los mismos.
Oligoelemento | Es necesario para… |
Hierro | Hemoglobina |
Zinc | Hormona insulina |
Cobre | Hemocianina |
Cobalto | Vitamina B12 |
Manganeso | Procesos fotosintéticos |
Litio | Neurotransmisores |
Silicio | Caparazones de diatomeas y rigidez de gramíneas |
Yodo | Hormona tiroidea |
Flúor | Esmalte dentario y huesos |
2. PRINCIPIOS INMEDIATOS Y BIOMOLÉCULAS
Son las moléculas que se obtienen en un análisis físico de la materia viva sin que se alteren las sustancias, mediante evaporación, filtración, destilación, diálisis, cristalización, electroforesis o centrifugación.
Simples | oxígeno molecular (O2) y nitrógeno molecular (N2) | |
Compuestos | Inorgánicos | agua, dióxido de carbono y sales minerales |
Orgánicos | glúcidos, lípidos, proteínas y ácidos nucleicos | |
Lo normal es que los bioelementos no se encuentren libres, sino que se unen entre sí mediante enlaces dando lugar a las biomoléculas.
![]()
![]() Los enlaces son las fuerzas de atracción que mantienen unidos a los átomos. En el caso de las biomoléculas, pueden ser fuertes (covalentes) y/o débiles (no covalentes). Los enlaces pueden ser:
Los enlaces son las fuerzas de atracción que mantienen unidos a los átomos. En el caso de las biomoléculas, pueden ser fuertes (covalentes) y/o débiles (no covalentes). Los enlaces pueden ser:
a) Iónicos: Uno de los átomos capta electrones del otro. Se da entre átomos de electronegatividad muy diferente (Ej.: NaCl)
b) Covalentes: Dos átomos comparten electrones. Los dos tienen electronegatividad alta y similar. Es un enlace muy fuerte. Se llama apolar si los dos átomos tienen electronegatividad similar (Ej.: CO2), y polar si un átomo atrae más hacia sí el par de electrones, formándose dipolos moleculares (Ej.: H2O).
c) Enlaces débiles/intermoleculares: Son enlaces entre moléculas.
• Enlaces de hidrógeno: Se da en moléculas en las que el H está unido a átomos muy electronegativos (O, N); esto confiere polaridad a la molécula. Las cargas + y – que se crean, se atraen estableciéndose este tipo de enlaces.
• Fuerzas de Van der Waals: Se producen por atracción electrostática entre los núcleos de una molécula y los electrones de otra. Estas fuerzas son mayores cuantos más electrones tienen las moléculas.
• Enlaces hidrofóbicos: Se da entre átomos que no tienen afinidad por el agua.
Los átomos de las moléculas biológicas suelen estar unidos por enlaces covalentes (formados al compartir entre ellos pares de electrones) constituyendo las moléculas sillares o monómeros (glucosa, aminoácidos, etc.). Estos monómeros, a su vez, se unen mediante enlaces también covalentes formando los polímeros. Los polímeros son moléculas complejas formadas por la unión de muchos monómeros (almidón, proteínas, etc.).
2.1. PRINCIPIOS INMEDIATOS INORGÁNICOS: EL AGUA
Es la sustancia más abundante en la materia viva (humanos 63% del peso). Existe una relación directa entre el contenido en agua y la actividad fisiológica de un organismo. En la materia viva se encuentra en tres formas:
– Agua circulante: sangre, savia…
– Agua intersticial: entre las células.
– Agua intracelular: en el citosol e interior de orgánulos.
Los organismos pueden conseguir el agua directamente, a partir del agua exterior o a partir de otras biomoléculas mediante reacciones químicas (agua metabólica).
CARACTERÍSTICAS DEL AGUA
Las propiedades fisicoquímicas del agua son consecuencia de su estructura química y de ellas derivan sus funciones biológicas.
– En la molécula del agua, el átomo de oxígeno comparte un par de electrones con cada uno de los átomos de hidrógeno siendo una molécula angulada.
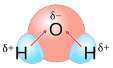 – Polaridad. Así, el núcleo del átomo de oxígeno, debido a su mayor electronegatividad, desplaza parcialmente a los electrones que constituyen los enlaces hacia su núcleo, dejando a los núcleos de los átomos de hidrógeno con una pequeña carga parcial positiva (δ+); mientras que existen regiones débilmente negativas (δ–) cerca del átomo de oxígeno. Por ello, la molécula de agua tiene en su estructura unas zonas con mayor densidad electrónica y otras con un déficit electrónico; lo que hace que sea una molécula dipolar.
– Polaridad. Así, el núcleo del átomo de oxígeno, debido a su mayor electronegatividad, desplaza parcialmente a los electrones que constituyen los enlaces hacia su núcleo, dejando a los núcleos de los átomos de hidrógeno con una pequeña carga parcial positiva (δ+); mientras que existen regiones débilmente negativas (δ–) cerca del átomo de oxígeno. Por ello, la molécula de agua tiene en su estructura unas zonas con mayor densidad electrónica y otras con un déficit electrónico; lo que hace que sea una molécula dipolar.
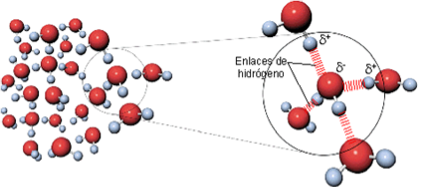
– Enlaces o puentes de hidrógeno. Como consecuencia de la estructura dipolar, las moléculas de agua pueden interaccionar unas con otras. Esta interacción se produce por atracción electrostática entre la carga parcial negativa del átomo de oxígeno de una molécula de agua y la carga parcial positiva localizada sobre los átomos de hidrógeno de otra molécula.
Debido a la ordenación de los electrones alrededor de los átomos de oxígeno, cada molécula de agua es potencialmente capaz de unirse mediante enlaces de hidrógeno a otras moléculas de agua, lo que permite que se formen estructuras de tipo reticular. Estos enlaces de hidrógeno entre las moléculas, se forman y escinden a una gran velocidad, aunque su estabilidad disminuye al elevarse la temperatura.
Los enlaces de hidrógeno mantienen unidas a las moléculas de agua entre sí, con lo que su peso molecular aumenta, y por ello, a una temperatura a la que otras moléculas químicamente comparables (H2S ó CH4) están en estado gaseoso, el agua se encuentra en estado líquido.
IMPORTANCIA BIOLÓGICA
a) Elevada fuerza de cohesión, debida a los puentes de hidrógeno; lo que explica que sea casi incompresible, capaz de dar volumen y turgencia a muchos seres vivos. Además, esta naturaleza cohesiva del agua es responsable de muchas de sus propiedades, tales como su elevada tensión superficial, elevada fuerza de adhesión (capilaridad), su elevado calor específico y su elevado punto de ebullición (calor de vaporización).
b) Elevada tensión superficial: la superficie opone una gran resistencia a romperse, lo que permite deformaciones en el citoplasma celular, causa los movimientos internos de la célula y posibilita el desplazamiento de algunos organismos sobre la superficie de medios acuáticos.
c) Capilaridad: adhesión de las moléculas de agua a las paredes de los conductos y entre sí, lo que permite la ascensión de la sabia bruta a través de los vasos leñosos
d) Elevado calor específico. Hace falta mucho calor para elevar su temperatura, lo que la convierte en un estabilizador térmico del organismo frente a los cambios bruscos de temperatura del ambiente.
e) Elevado calor de vaporización. Para pasar de líquido a gas hay que romper todos los puentes de hidrógeno existentes en la fase líquida. Esta propiedad, junto con la anterior, participa en el proceso de amortiguación térmica, pues se consigue una disminución de la temperatura de un organismo al perder una cantidad de calor que es empleada en la evaporación del agua. La sudoración es un método fisiológico de refrigeración, basado en esta propiedad.
f) Densidad máxima en estado líquido a los 4 oC, lo que explica que el hielo flote y forme una capa superficial en charcos, ríos, etc. que permita la vida bajo ella. Si el hielo fuera más denso, acabaría helándose toda el agua.
g) Elevada constante dieléctrica. Al ser dipolar, el agua es un gran disolvente de compuestos iónicos (ej. sales) y covalentes polares (ej. glúcidos).
El proceso de disolución se debe a que las moléculas de agua, al ser polares, se disponen alrededor de los grupos polares del soluto, llegando en el caso de los compuestos iónicos a desdoblarlos en aniones y cationes, que quedan así rodeados por moléculas de agua. Este fenómeno se llama solvatación iónica.
Con esto se deduce que una de las primordiales funciones del agua es la de actuar como disolvente de la mayoría de las moléculas, y dado que es condición imprescindible que para que una reacción química tenga lugar, los reactivos se encuentren disueltos, podemos deducir que el agua, al permitir la disolución de los compuestos biológicos, actúa como el medio donde se realizan todas las reacciones metabólicas características de la actividad vital.
Así mismo, sirve de vehículo de entrada y salida de las distintas sustancias disueltas en ella, a través de la membrana, en la célula.
h) Bajo grado de ionización. Una pequeña parte de las moléculas de agua puede ionizarse al unirse un átomo de hidrógeno de una molécula al oxigeno de otra molécula, rompiendo su unión con la primera. Aparecen así, dos iones de carga opuesta: H3O+ y OH–.
H2O + H2O → H3O+ + OH–
pH = –log [H+]
(Habitualmente, los iones H3O+ se representan con H+)
En el agua destilada, la proporción de moléculas ionizadas es muy baja:
A 25 oC, [H+] ∙ [OH–] = 1 ∙ 10-14 → A este producto se le denomina producto iónico del agua.
Dados estos bajos niveles, si al agua se le añade un ácido (H3O+) o una base (OH–), aunque sea poca cantidad, estos niveles varían bruscamente. De esta propiedad deriva la función del agua como reguladora del pH en el medio orgánico.
FUNCIONES DEL AGUA EN LOS SERES VIVOS
- Función disolvente.
- Función bioquímica. El agua interviene en muchas reacciones químicas.
- Función de transporte.
- Función estructural. Da volumen y forma a las células. Esqueleto hidrostático en plantas e invertebrados.
- Función mecánica amortiguadora. En articulaciones en vertebrados (líquido sinovial).
- Función termorreguladora. Debida a su elevado calor específico y de vaporización.
- Función reguladora del pH.
2.2. PRINCIPIOS INMEDIATOS INORGÁNICOS: LAS SALES MINERALES
Se pueden encontrar en tres formas:
a) Sustancias minerales precipitadas. En forma precipitada, las sales minerales, forman estructuras sólidas insolubles, que proporcionan estructura (función esquelética) o protección al ser que las posee.
Ejemplos: carbonato cálcico (Ca2CO3) en caparazones de algunos protozoos marinos, esqueletos externos de corales, moluscos y artrópodos; fosfato cálcico (Ca3(PO4)2) en esqueletos de vertebrados; silicatos en los caparazones de las diatomeas, las espículas de las esponjas y las estructuras de sostén de algunas gramíneas.
b) Sales minerales disueltas. Las sales disueltas en agua, están ionizadas, es decir, manifiestan cargas positivas (cationes) o negativas (aniones). Los cationes más abundantes en la composición de los seres vivos son Na+, K+, Ca2+, Mg2+, NH4+. Y los aniones más representativos son Cl–, PO43-, CO32-, HCO3–. Las sales disueltas en agua pueden realizar funciones tales como:
- Mantener el grado de salinidad.
- Controlar la contracción muscular.
- Producir gradientes electroquímicos.
- Estabilizar dispersiones coloidales.
- Intervienen en el equilibrio osmótico. Cada ión desempeña funciones distintas y, a veces, antagónicas. Ej.: el K+ aumenta la turgencia de la célula y el Ca2+ la disminuye. Son iones antagónicos.
- Amortiguar cambios de pH, mediante el efecto tampón. Este fenómeno consiste en contrarrestar el efecto de los ácidos o bases añadidos a una disolución. A las disoluciones capaces de hacer esto, se las llama disoluciones tampón o amortiguadoras.
Los líquidos biológicos consiguen mantener su pH estable, debido a que contienen ciertas sales minerales que pueden ionizarse para dar lugar a H3O+ o a OH– que contrarresten el exceso de uno u otro ion añadido.
Un ejemplo es el sistema tampón fosfato (intracelular): H2O + H2PO4– ↔ HPO42- + H+
Si en la célula aumentara la acidez (H+), la reacción se desplazaría a la izquierda; y si disminuyera, hacia la derecha. Así, se amortiguarían las variaciones.
Otro ejemplo es el sistema tampón bicarbonato (extracelular):
CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3–
c) Sustancias minerales asociadas. Se asocian a moléculas orgánicas tales como proteínas (fosfoproteínas), lípidos (fosfolípidos) y glúcidos (agar – agar) realizando funciones que tanto el ion como la molécula no realizarían por separado.
FUNCIONES DE LAS SALES MINERALES
1) Formar estructuras esqueléticas.
2) Regular el balance del agua dentro y fuera de las células (electrolitos) ⇒ Ósmosis.
3) Intervenir en la excitabilidad nerviosa y en la actividad muscular (calcio, magnesio).
4) Permitir la entrada de sustancias a las células (la glucosa necesita del sodio para poder ser aprovechada como fuente de energía a nivel celular).
5) Colaborar en procesos metabólicos (el cromo es necesario para el funcionamiento de la insulina, el selenio participa como un antioxidante).
6) Intervenir en el buen funcionamiento del sistema inmunológico (zinc, selenio, cobre).
7) Estabilizar dispersiones coloidales.
8) Mantener un grado de salinidad en el medio interno.
9) Constituir disoluciones amortiguadoras de pH.
3. DISOLUCIONES Y DISPERSIONES COLOIDALES
En estado líquido en los seres vivos tenemos:
– Soluto: muchos tipos de moléculas dispersas.
– Disolvente: un solo tipo de fase dispersante → el agua.
Los solutos pueden ser de bajo peso molecular (cristaloides) o de alto (coloides). Las dispersiones de solutos de bajo peso molecular se llaman verdaderas y las de alto, coloidales.
3.1. PROPIEDADES DE LAS DISOLUCIONES VERDADERAS
a) Difusión: repartición homogénea de las partículas de un fluido en el seno de otro, al ponerlos en contacto. Se debe al continuo movimiento de las partículas. Ej.: alveolos.
b) Ósmosis: paso del disolvente entre dos soluciones de diferente concentración a través de una membrana semipermeable que impide el paso de las moléculas de soluto.
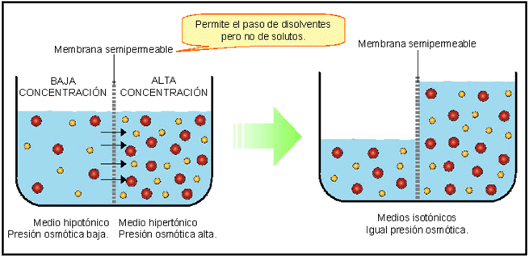
Si una membrana como la descrita separa un líquido en dos particiones, una de agua pura y otra de agua con azúcar, dado suficiente tiempo, parte del agua de la zona sin azúcar habrá pasado a la de agua con azúcar. El agua pasa de la zona de baja concentración a la de alta concentración.
Las moléculas de agua atraviesan la membrana semipermeable desde la disolución de menor concentración (disolución hipotónica), a la de mayor concentración (disolución hipertónica). Cuando el trasvase de agua iguala las dos concentraciones, las disoluciones reciben el nombre de isotónicas.
En los seres vivos, este movimiento del agua a través de la membrana celular puede producir que:
– En un medio hipertónico, las células se arruguen (retracción) por una pérdida excesiva de agua, y si no llegan a igualarse las concentraciones dentro y fuera de la célula, sufran plasmólisis.
– En un medio hipotónico, las células se hinchen (turgencia) por un aumento también excesivo en el contenido celular de agua; y si no se llegan a igualar las concentraciones, se produzca el estallido celular.
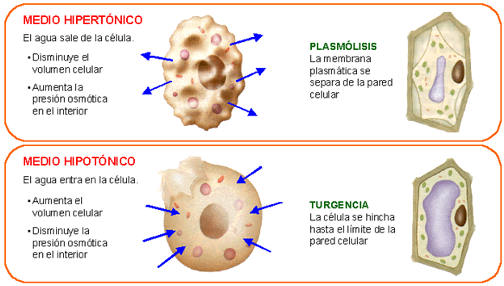
Para evitar estas dos situaciones, de consecuencias desastrosas para las células, éstas poseen mecanismos para expulsar el agua o los iones mediante un transporte que requiere gasto de energía.
c) Estabilidad del grado de acidez o pH: como hemos visto antes, el pH es el logaritmo decimal cambiado de signo de la concentración de iones hidronio. Sus valores oscilan entre 0 y 14, siendo de 0 a 7 una disolución ácida, 7 será neutra, y de 7 a 14 será una disolución básica.
Las sales minerales disueltas mantienen constante el pH del medio interno de los seres vivos gracias al papel que juegan como disoluciones tampón.
3.2. LAS PROPIEDADES DE LAS DISPERSIONES COLOIDALES
a) Capacidad de presentarse en estado de gel. Se pueden presentar en dos estados: en forma de sol (líquido) o de gel (semisólido y gelatinoso). Estos estados se alternan debido a variaciones de temperatura, pH, presión o concentración.
En el estado sol, las moléculas de soluto se encuentran en menor proporción que las de la fase dispersante líquida.
En el estado gel, las moléculas de disolvente están atrapadas entre las de soluto, que se entrelazan formando una red continua que actúa como fase dispersante. La red impide que el disolvente fluya, por lo que el gel se comporta como un sólido blando y fácil de deformar. Ej.: pectinas de frutas, gelatina y colágeno.
Del estado de sol se puede pasar al de gel, pero no siempre el proceso es reversible. La transformación de sol en gel y viceversa, está en relación con la síntesis o con la despolimerización, respectivamente, de proteínas fibrilares.
b) Elevada viscosidad: resistencia interna que presenta un líquido al movimiento relativo de sus moléculas. Las dispersiones coloidales, dado el gran tamaño de sus moléculas (mayor de 10-7 cm), son muy viscosas.
c) Elevado poder adsorbente: atracción que ejerce la superficie de un sólido sobre las moléculas de un líquido o de un gas. La misma cantidad de sustancia ofrece mayor adsorción si se encuentra finamente dividida. No hay que confundir con absorción, donde las moléculas penetran en el sólido.
d) Efecto Tyndall. Las dispersiones coloidales, al igual que las disoluciones verdaderas, son transparentes y claras. Pero si se iluminan lateralmente y sobre fondo oscuro, se observa una cierta opalescencia provocada por la reflexión de los rayos luminosos.
e) Sedimentación. Las dispersiones coloidales son estables en condiciones normales, pero si se someten a fuertes campos gravitatorios, se puede conseguir que sedimenten sus partículas.
f) Diálisis: separación de las partículas dispersas de elevado peso molecular de las de bajo peso molecular, gracias a una membrana de diálisis (semipermeable). Una aplicación clínica es la hemodiálisis.
g) Electroforesis: transporte de las partículas coloidales gracias a la acción de un campo eléctrico a través de un gel.